

استقرار الأدوية هو واحد من أهم التحديات في صناعة الأدوية. تتراوح المنتجات الصيدلانية من الأدوية المصنعة كيميائيًا للجزيئات الصغيرة إلى البيولوجية المعقدة المستمدة من الكائنات الحية أو عمليات التكنولوجيا الحيوية. بسبب خصائصها الفيزيائية والكيميائية المختلفة ، تستجيب هذه الأدوية بشكل مختلف تمامًا لتغيرات درجة الحرارة.

في الاختبارات الصيدلانية والتخزين ، درجة الحرارة ليست حالة خلفية-إنها عامل استقرار رئيسي يؤثر بشكل مباشر على سلامة الدواء وفعاليته وعمر الصلاحية.
الأدوية البيولوجية حساسة بشكل خاص لدرجة الحرارة بسبب هياكلها القائمة على البروتين:
زيادة طفيفة في درجة الحرارة قد يسبب تمسخ البروتين
التشوه الهيكلي يمكن أن يؤدي إلى فقدان النشاط الدوائي
بمجرد التشويه ، غالبًا ما يكون النشاط البيولوجي لا رجعة فيه
حتى الانحرافات الطفيفة في درجة الحرارة أثناء الاختبار أو التخزين يمكن أن تؤثر على فعالية المنتج.
بالنسبة لبعض المستحضرات السائلة ، يمكن أن تشكل درجات الحرارة المنخفضة للغاية مخاطر:
المغلفات قد تتبلور في ظروف درجات الحرارة المنخفضة
يمكن أن تتغير نسب التركيز ، مما يؤثر على دقة الجرعة
التبلور قد يمنع إبر الحقن ويزيد من خطر المريض
تسلط هذه القضايا الضوء على ضرورة بيئات درجة الحرارة الخاضعة للرقابة والمتكررة أثناء تقييم الاستقرار.
تتعرض الأدوية المصممة للتخزين على المدى الطويل باستمرار لتغيرات درجة الحرارة البيئية أثناء التخزين والنقل والمناولة اليومية. بمرور الوقت ، يمكن لدورات درجة الحرارة الصغيرة والمتكررة أن تعمل كعامل تدهور تراكمي ، مما يؤدي إلى:
التدهور الكيميائي
زيادة مستويات النجاسة
انخفاض الفعالية العلاجية
وهذا يجعل التحكم في درجة الحرارة ضمانة للجودة على المدى الطويل ، وليس مجرد شرط اختبار على المدى القصير.
أثناء تطوير الأدوية في وقت مبكر ، لا يمكن تجنب عدم اليقين.غرف درجة الحرارةهي أدوات أساسية لفحص الصياغة ومقارنة الاستقرار في هذه المرحلة.

تشمل التطبيقات النموذجية في R & D:
تقييم سلوك الصياغة تحت ضغط درجات الحرارة العالية والمنخفضة
محاكاة دورات درجات الحرارة اليومية أو الموسمية
مقارنة الاستقرار الهيكلي عبر عدة مرشحين مجمع
من خلال مراقبة التغيرات الفيزيائية والكيميائية في ظل ظروف درجة الحرارة التي يتم التحكم فيها ، يمكن للباحثين تحديد التركيبات ذات الهياكل الثابتة والأداء الموثوق به ، مما يوفر أساسًا قويًا لمزيد من التطوير.
غرفة اختبار درجة حرارة عالية منخفضةتظل لا غنى عنها في جميع عمليات تصنيع الأدوية وضمان الجودة.
يتم تقييم المواد الخام الواردة بشكل روتيني في ظروف درجة الحرارة التي يتم التحكم فيها. على سبيل المثال ، قد تختلف جودة كبسولة الجيلاتين بسبب الاختلافات في درجة الحرارة أثناء المعالجة الأولية. تساعد غرف درجة الحرارة على التحقق مما إذا كان الجيلاتين يحافظ على أداء التبلور المتسق في ظروف درجات الحرارة القياسية والقاسية قبل الموافقة عليه للاستخدام في الإنتاج.
في إنتاج المضادات الحيوية ، تؤثر درجة حرارة التخمير بشكل مباشر على اتساق المكونات النشطة. حتى الانحرافات الطفيفة في درجات الحرارة يمكن أن تؤدي إلى تقلب الدفعة. عن طريق محاكاة سيناريوهات مختلفة لدرجة حرارة التخمير في أغرفة درجة حرارة ثابتة، يمكن للمصنعين:
تحليل تأثير درجة الحرارة على إنتاجية المكونات النشطة
تحسين معلمات العملية
ضمان الاتساق من الدفعة إلى الدفعة
التحقق من صحة هذه العملية ضروري للحفاظ على جودة الدواء مستقرة على نطاق واسع.
تستمر غرف درجة الحرارة في لعب دور حيوي بعد دخول الأدوية إلى السوق. وفقًا للمتطلبات التنظيمية ، تجري شركات الأدوية بشكل روتيني دراسات استقرار ما بعد التسويق باستخدام عينات السوق.
تتضمن هذه الدراسات عادة:
التعرض طويل الأجل في ظل ظروف التخزين الخاضعة للرقابة
اختبار دوري لنمو الشوائب وفقدان الفعالية
جمع البيانات للتفتيش والتدقيق التنظيمي
في حالة اكتشاف حالات تشوهات ، يمكن للشركات المصنعة تعديل توصيات التخزين أو الشروع في اتخاذ إجراءات تصحيحية على الفور ، مما يقلل من المخاطر التي تهدد سلامة المرضى.
يعتمد تقييم الاستقرار الصيدلاني في المقام الأول على نهجين اختبار تكميليين.
يحاكي اختبار الثبات السريع شيخوخة الدواء على المدى الطويل خلال إطار زمني أقصر من خلال تطبيق درجة حرارة مرتفعة وظروف رطوبة خاضعة للتحكم.
تتضمن الأهداف النموذجية ما يلي:
التنبؤ بمسارات التدهور المحتملة
تقدير مدة الصلاحية أثناء التطوير المبكر
دعم صياغة قرارات الفرز
تعمل هذه الطريقة بشكل كبير على تحسين كفاءة R & D مع توفير بيانات تنبؤية قيمة.
يسجل اختبار الاستقرار على المدى الطويل التغييرات في الوقت الفعلي في ظل ظروف قريبة من بيئات التخزين الفعلية. هذه البيانات ضرورية لما يلي:
تحديد تواريخ انتهاء الصلاحية بدقة
تحسين ظروف التخزين والنقل
دعم التقارير والموافقات التنظيمية
يتم إجراء دراسات الاستقرار الصيدلاني ضمن أطر تنظيمية راسخة لضمان موثوقية البيانات والقبول العالمي. تشمل الإرشادات المرجعية الشائعة ما يلي:
ش Q1A(R2)-اختبار استقرار المواد والمنتجات الدوائية الجديدة
ش Q1B-اختبار الاستقرار الضوئي للمواد والمنتجات الدوائية الجديدة
GMPمتطلبات التحكم البيئي وإمكانية تتبع البيانات
يجب أن تدعم غرف درجة الحرارة المستخدمة في الاختبارات الصيدلانية الظروف المستقرة والتكرار وسجلات البيانات الكاملة لتلبية هذه التوقعات التنظيمية.
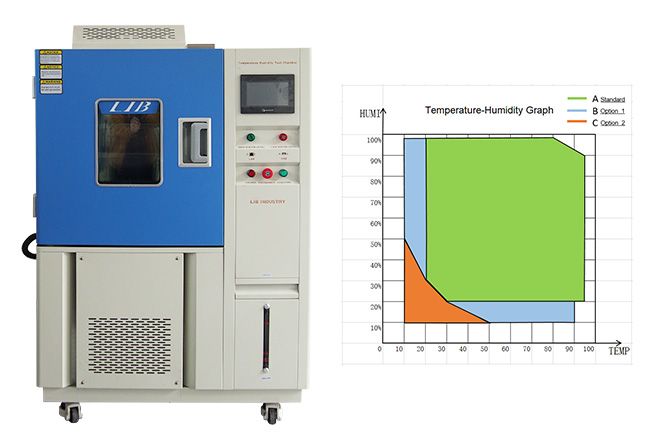
لاختبار الاستقرار الصيدلاني ، توفر غرف درجة الحرارة عمومًا خصائص الأداء التالية:
نطاق درجة الحرارة:-20 درجة مئوية إلى 60 درجة مئوية(قابل للتخصيص)
تذبذب درجة الحرارة:± من من من
التوحيد درجة الحرارة:± 2 درجة مئوية
أوضاع الاختبار: الاستقرار المتسارع والاستقرار على المدى الطويل
تسجيل البيانات: التسجيل المستمر للتدقيق والامتثال
تضمن هذه المعلمات ظروف تعرض ثابتة ونتائج اختبار موثوقة.
توفر غرف درجة حرارة صناعة LIB بيئات درجة حرارة ثابتة وقابلة للتكرار لاختبار الاستقرار الدوائي.
تذبذب درجة الحرارة: ± + درجة مئوية
توحيد درجة الحرارة: ± 2 درجة مئوية
يدعم: دراسات الاستقرار المتسارعة وطويلة الأجل
تسجيل البيانات: سجلات درجة الحرارة والرطوبة المستمرة
نموذج | T-100 | T-225 | T-500 | T-1000 |
حجم داخلي | 100 لتر | 225 لتر | 500 لتر | 1000 لتر |
الحمل الحراري | ، دبليو | |||
نطاق درجة الحرارة | أ: -20 ℃ ~ ، ℃ ب: -40 ℃ ~ ، ℃ ج: -70 ℃ ~ ، ℃ | |||
تذبذب درجة الحرارة | ± ، ℃ | |||
انحراف درجة الحرارة | ± ، ℃ | |||
معدل التبريد | 1 ℃/دقيقة | |||
معدل التدفئة | 3 ℃/دقيقة | |||
نظام التبريد | مبرد صديق للبيئة ، ضاغط تيكومسيه فرنسي ، متوافق مع متطلبات معايير GWP | |||
وحدة تحكم | وحدة تحكم بشاشة تعمل باللمس LCD ملونة قابلة للبرمجة ، اتصال إيثرنت | |||
 | ||||
تساعد هذه القدرات الشركات المصنعة للأدوية على توليد بيانات استقرار موثوقة وتقليل انحراف الاختبار وتلبية متطلبات الفحص التنظيمي بثقة.
تدعم غرف درجة حرارة صناعة LIB برامج البحث و الاستقرار والتصنيع وما بعد التسويق الصيدلانية من خلال الجمع بين التحكم الدقيق في درجة الحرارة والتصميم الموجه نحو الامتثال ، وسجلات بيانات قابلة للتتبع-مساعدة الشركات المصنعة على حماية جودة المنتج وسلامة المريض طوال دورة حياة المنتج بالكامل.
الاتصال صناعة ليبInquiry@libtestchamber.comللحصول على توافقحجرة درجة الحرارةحل في غضون 1 إلى 3 ساعات لاختبار الاستقرار الصيدلاني عبر برامج R & D والإنتاج والاستقرار.
 English
English русский
русский français
français العربية
العربية Deutsch
Deutsch Español
Español 한국어
한국어 italiano
italiano tiếng việt
tiếng việt ไทย
ไทย Indonesia
Indonesia


